El estudio del átomo ha sido el centro de la preocupación de muchos científicos desde antes de Cristo, cuyos estudios que han derivado en una serie de modelos atómicos que explican su conformación y funcionamiento, como el modelo atómico de John Dalton, (1766-1844), científico británico quien hizo grandes aportes a la ciencia, no solo en química, sino también en física y matemáticas.
Contenido
¿Qué es un modelo atómico?
Antes de profundizar en lo que es un modelo atómico y en el modelo atómico de Dalton, se debe conocer qué es un átomo.
Átomo es una palabra griega que significa indivisible; y el átomo “es la unidad más básica de la materia con propiedades de un elemento químico; es el componente fundamental de toda la materia, es decir, todo lo que está en el universo está conformado por átomos, así como todo el universo, las estrellas, planetas, galaxias y los cuerpos cósmicos”.
Los átomos se agrupan formando moléculas y las moléculas constituyen todos los materiales que se conocen, con las características químicas y físicas que podemos ver.
Un modelo atómico es la representación simbólica o gráfica del átomo, por medio del cual se describe la clase de átomo y el número de partículas fundamentales que lo componen, y explica la forma como se comportan y organizan.
Entre los modelos atómicos propuestos está el de John Dalton, el primero en tener una base científica, y que tuvo su punto de partida en el aporte que había hecho Demócrito, en el siglo IV antes de Cristo.
Es decir que la primera referencia que se tiene del átomo la ofreció el filósofo griego Demócrito, conocido como el “filósofo que ríe”, quien consideró al átomo como la partícula más pequeña y sin división de la materia.
Los postulados de esta teoría, así como todas las teorías filosóficas griegas, no están sustentados en experimentos, sino que son explicadas a través de razonamientos lógicos, y en cuanto a las ideas de Demócrito surgieron de sí mismo por meditación e intuición, llegando a la conclusión de que el átomo es la partícula más pequeña de la materia, indivisible e indestructible.
¿Cuáles son los postulados de Dalton?
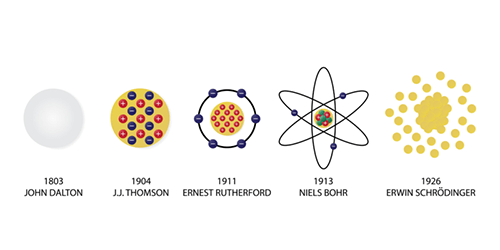
Algunos modelos atómicos aportaron elementos para la estructura del átomo actual, como la que en 1803, en Inglaterra, explicó John Dalton, científico británico quien presentó una serie de leyes hasta entonces desconocidas que se consideraron en la teoría atómica moderna, y que sirven para explicar la ley de la conservación de la masa, la ley de la composición constante y la ley de las proporciones múltiples, del mismo Dalton.
John Dalton centró las primeras bases sobre la Teoría atómica mediante la cual se logra demostrar que el átomo es indivisible y presenta una estructura interna. Imaginó que los átomos eran como esferas compactas con tamaños y masas diferentes.
En 1803, específicamente en el mes de agosto, gracias a sus descubrimientos, John Dalton dio a conocer públicamente la formulación de su teoría atómica en una conferencia que se llevó a cabo en Manchester, organizada por la Sociedad Literaria y Filosófica de la cual formaba parte el científico inglés y a la que solo asistieron siete personas.
Según los historiadores, la exigua asistencia fue debido a la fama de Dalton de ser un mal expositor; no obstante, captó el interés de más gente cuando en 1808 publicó su libro Nuevo sistema de filosofía química, como se denominaba la primera parte de la obra.
Postulados de Dalton
- El modelo atómico de Dalton se puede resumir sobre la base de una serie de postulados simples, como que la materia se conforma de partículas diminutas que llevan por nombre átomos, los cuales no se pueden dividir y son indestructibles en cualquier reacción química.
- También aclara que los átomos que pertenecen a una misma sustancia que no puede ser descompuesta en otras más simples son iguales entre sí, por lo que poseen la misma masa y características, por ejemplo todos los átomos de hidrógeno son iguales.
- La materia está constituida en su totalidad a partir de átomos que no se pueden ni generar ni destruir.
- Las características de los átomos de diferentes elementos siempre son diferentes, y poseen distintas características.
- En todos los casos, los átomos de un elemento concreto tienen el mismo peso, tamaño y cualidades, y todos ellos son iguales entre sí.
- Si bien pueden combinarse con otras sustancias para formar diferentes compuestos, los átomos en sí permanecen inalterables, y no pueden ser divididos ni destruidos.
- Los compuestos se forman mediante la combinación de los átomos de dos o más elementos diferentes.
- La combinación entre dos elementos determinados resulta en compuestos diferentes de acuerdo con las proporciones en las que se mezclen.
- Un mismo compuesto es producido siempre por una misma proporción en la combinación de los átomos.
- La combinación de diferentes tipos de átomos realiza mediante relaciones simples.
- En las reacciones químicas suceden transformaciones, creaciones y disgregaciones de moléculas, y son el resultado de una reorganización de los átomos que están presentes en cada compuesto.
Errores del modelo atómico de Dalton
Con el avance de la ciencia, los estudios y los nuevos conocimientos que se continuaron y se generaron acerca del átomo lograron demostrar que a pesar de que la teoría atómica de Dalton ha sido de gran relevancia para la ciencia en cuanto a desentrañar la conformación de la materia, algunos de sus postulados son refutables.
Como por ejemplo, se ha demostrado que es un error lo dicho por Dalton que “el átomo es una unidad indivisible”, pues se ha podido identificar a los protones, neutrones y electrones dentro del átomo, identificadas como estructuras subatómicas.
Así mismo, se demostró que es un error el postulado de “todos los átomos de una misma sustancia tienen iguales propiedades”, ya que se encontraron átomos con carga eléctrica diferente, dependiendo del total de protones y electrones, conocidos como iones, y los isótopos, con diferentes masas atómicas.
Otro aspecto que ha quedado evidenciado ser distinto al postulado del modelo atómico de Dalton es la teoría de que los átomos no se modifican, lo cual fue demostrado a partir de la fisión y fusión nuclear.
Aun cuando las nuevas investigaciones han demostrado que varios postulados de Dalton no son del todo ciertos, el modelo atómico de Dalton sirvió para avanzar en la química moderna y permitió un desarrollo relevante en el estudio y entendimiento de la materia, su transformación y comportamiento.

